-1.png)
あーこの患者さん腎機能悪いのにファモチジンが減量されてない……この患者さんはファモチジンを飲んでるのにファモチジンの注射オーダーが出ている……どっちも主治医に確認しなきゃ

意外と多い事例であるな。胃薬だから気にされにくいのかもしれない
-1.png)
たしかに……! 別に胃薬だしちょっとぐらい多くても良いですかね?

いや、ファモチジンをはじめ胃薬の過量投与には恐ろしいリスクが潜んでいるのであるよ
-1.png)
いやー胃薬ですよ? 過量投与してもむしろ胃の調子が良くなるだけじゃないですか?

ほほう。たかが胃薬、されど胃薬。どんなリスクがあるか、勉強していこう
もくじ
H2受容体拮抗薬と腎機能と過量投与とそのリスク
H2受容体拮抗薬とは胃粘膜壁細胞にあるH2受容体を遮断して胃酸分泌を抑制することにより、胃・十二指腸潰瘍、胃炎等に用いられる薬です。
今回はその中でも一般的に使用頻度が高いと考えられるファモチジンを例として色々考えてみましょう。
ファモチジンは主に腎臓より未変化体のまま排泄されるため、腎機能障害患者では血中濃度が高値で持続することが知られています。通常は血中消失半減期が2.6時間程度なのに対し、腎機能障害がある場合は有意に延長し10時間を超えることも(表1)。
体内に取り込まれた薬の量を示すAUC(血中濃度-時間曲線下面積)も表の通り上昇します。
そのため、ファモチジンを腎機能障害患者に投与する際には腎機能に応じた用量調節が必要とされるのです。添付文書には腎機能に応じた用量調節表(表2)が載っているので、用量決定の際の参考にすることができるでしょう。
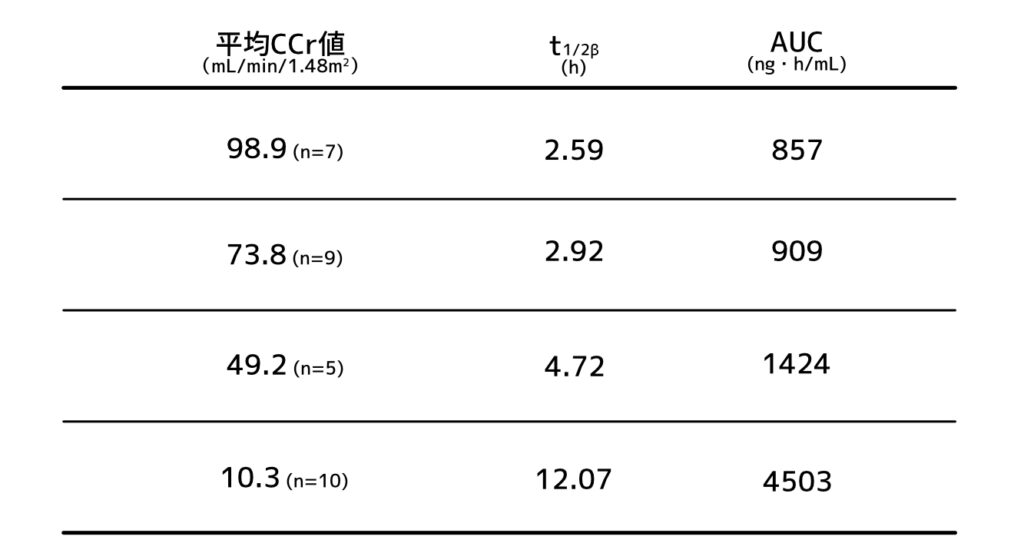
表1 ファモチジン20mgを静脈内投与したときのパラメータ(ガスター錠添付文書より作成)

表2 腎機能低下患者への投与法(ガスター錠 添付文書より作成)
-1.png)
でも腎機能が悪いのに常用量で処方が出ることもしばしば……やっぱり胃薬なので少しくらい多くてもむしろ胃の調子が良くなるだけなんじゃないですか?

たしかに腎機能の数字を見た画一的な対処ではなく薬効とリスクの兼ね合いを考えることは大事なのだが……はたしてこの場合はどうだろうか
薬剤師うさぎの言うように胃薬なので少しくらい量が多くても別に問題ないでしょうか?
ここでたまに現場で起こりうる議論である、添付文書や書籍に載っている用量調節表はきっちりと守らねばならないか否かということについて考えてみましょう。
例えば、もともと腎機能がCCr60ml/min程度だったのが少し数値が低下してCCr59ml/minになった場合はどうでしょうか。用量調節表に従うとこの場合は用量を半分にする必要がありそうですが、腎機能はいきなり半分になるわけではありません。
腎排泄型薬剤の場合、CCrと腎クリアランスは相関し徐々に低下するため、この場合は厳密に用量調節表に従って今すぐ投与量を半減する必要性は必ずしも大きくなさそうです。
これは別に添付文書なんて従うなかれというアウトロー思考を推奨しているわけではありません。数値だけを見て画一的に減量するのではなく、患者さんを見て薬の効果はどうか、副作用は出ていないかなど のリスク(害)とベネフィット(益)をそれぞれ考えた対応が大切なのです。
さて、そのためにはまず薬のリスクを知る必要があります。腎機能に応じてH2受容体拮抗薬の投与量を減量しなかった場合、薬物有害反応の発生リスクは2~4倍に増加するという報告がありました1)。
それではH2受容体拮抗薬が過量投与されることによるリスクについて一つずつ見ていきましょう。

まずは精神錯乱、幻覚症状、痙攣、せん妄などの中枢神経障害が挙げられよう
-1.png)
胃薬で……せん妄?
まずH2受容体拮抗薬はそれ自体がせん妄ハイリスク薬に該当します。
特に高齢者に対するH2受容体拮抗薬の投与はせん妄や認知機能低下を引き起こすリスクがあるため、可能な限り控えることが推奨されています2)。
ヒスタミンは中枢神経系において覚醒を司る神経伝達物質であるため、ヒスタミン受容体の遮断は覚醒レベルの低下を来す可能性があります。
H2受容体は視覚や聴覚に関与する大脳皮質や短期記憶に関与する海馬に存在しているため、拮抗によりせん妄や幻覚など中枢神経系の症状が起こるものと考えられているようです3)。
ファモチジンの静注により中枢神経障害をきたした血液透析患者において脳脊髄液中の薬物濃度が著明に上昇していたことが報告されており、ファモチジンの蓄積が中枢神経系副作用の発現と関連していることが示唆されています4)。
実際に、ファモチジンにより抑うつとせん妄を呈した症例5)や、末期癌患者のせん妄にファモチジンの関与が示唆された症例6)などファモチジンによる中枢神経系の副作用を疑う症例などが報告されています。
この中枢神経系の副作用の発生頻度は一般的に投与開始後2週間以内で高く、投与を中止することで3日以内に回復するとされており7)、特に高齢者や腎機能障害のある患者では投与開始後の状態を注意深くモニタリングすることが重要でしょう。

汎血球減少、再生不良性貧血などの血液障害も
-1.png)
胃薬で…………血液障害?
正確なメカニズムは解明されていないようですが、in vitroにおいてH2受容体遮断薬のシメチジンが骨髄のH2受容体に強い阻害効果があることが報告されており8)、造血機能への影響が推察されます。
実際に透析患者へのファモチジンの投与により汎血球減少が疑われた症例9)などが報告されています。
その他、Torsades de pointesのリスク上昇が報告されていたり10)、間質性腎炎11)、薬剤性パーキンソニズム12)などファモチジンが被疑薬とされる副作用が報告されています。
また、PPIなども含めた胃酸分泌抑制薬の長期投与による全般的なリスクとしてビタミンB12欠乏、低マグネシウム血症、腎障害、肺炎、認知症、Clostridioides difficile感染症などにも関連することが指摘されています3)。
-1.png)
たかが胃薬といえどいろんなリスクがあるんですね……。ところで投与量を減量することでそもそもの胃薬としての効果が発揮できなくなってしまう……ってことはないんですか?

たしかに良かれと思って減量した結果、薬の効果が弱くなって消化管出血などが起きたらそれは由々しき事態であるが……
上述したように腎機能の程度に応じて投与量を調節する際は、減量によるリスクとベネフィットを考慮する必要があります。
ファモチジンを含むH2受容体拮抗薬のリスクは、これが全てとは限りませんがこれまで記載したようなものを想定できれば良いでしょう。
一方ベネフィットは胃腸障害や消化管出血の抑制であり、それらの症状は胃内のpHを4、または5.4以上に保つことで予防できることが示唆されています13),14)。
薬による胃酸の分泌抑制がどのくらい胃内pHを上昇させるのかについて、健常成人にファモチジン20mgを1回経口投与すると、1時間後には胃内pHは4以上になり12時間後まで5~6の範囲で推移することがわかっています15)。
これらを念頭に置くと薬の効果としては健常成人に対しては1回20mgの投与で十分であることが推察されます。腎機能の低下した患者に対してもその腎機能に応じて投与量を調節し、同等の血中濃度を保つことができれば効果は十分期待できると考えて良いでしょう。
実際に投与量を腎障害に合わせて変更することが消化管疾患のコントロールに影響を与えるかどうかについて後方視的に検討した観察研究があります。
この報告ではニザチジンの投与量を腎機能に応じて調節した群と調節しなかった群に分けており、結果としては疾患コントロールはどちらの群でも同様で、消化管出血イベントも同程度であったと報告されていました16)。
これらのことから減量による効果の減弱をあまり恐れる必要はなさそうです。
また、医療費の削減という観点からも腎機能に応じた減量のメリットがあり、高齢者の腎機能を考慮してH2受容体拮抗薬の投与量を調整すると総薬剤費が10%減少するという報告がありました17)。
まとめ
-1.png)
たかが胃薬といえどいろんなリスクがあるんですね……

過度にリスクを危惧して肝心の治療のほうがおろそかになってしまうのは良くないが、単純な重複だったり腎機能が考慮されていなかったり不必要に長期継続されていたりする場合は積極的に介入すべきであろうぞ
-1.png)
リスクとベネフィットを考えるということですね。色々考えられるように努力しようと思います……!
参考文献
(1)J Manlucu et al :Dose-reducing H2 receptor antagonists in the presence of low glomerular filtration rate: a systematic review of the evidence, Nephrol Dial Transplant. 2005 Nov;20(11):2376-84.
(2)日本老年医学会編:高齢者の安全な薬物療法ガイドライン2015, メジカルビュー, 2015
(3)クリティカルケア薬
(4)K Yoshimoto et al : Famotidine-associated central nervous system reactions and plasma and cerebrospinal drug concentrations in neurosurgical patients with renal failure, Clin Pharmacol Ther. 1994 Jun;55(6):693-700.
(5)星越活彦:famotidineにより抑うつとせん妄を呈した症例, 臨床精神医学 29(12) : 1617-1623, 2000
(6)冨安志郎ほか:末期癌患者のせん妄にファモチジンの関与が示唆された症例, 日本ペインクリニック学会誌 8 (2) 55-55, 2001.
(7)T G Cantú , J S Korek, Central nervous system reactions to histamine-2 receptor blockers, Ann Intern Med. 1991 Jun 15;114(12):1027-34.
(8)J.W. Byron:CIMETIDINE AND BONE-MARROW TOXICITY, Lancet 10 555-556, 1977
(9)川上美由希ほか:Famotidineの蓄積による汎血球減少症が疑われた2透析症例, TDM研究 17(2): 133-134, 2000.
(10)Elisabetta Poluzzi et al : Drug-induced torsades de pointes: data mining of the public version of the FDA Adverse Event Reporting System (AERS), Pharmacoepidemiol Drug Saf. 2009 Jun;18(6):512-8.
(11)K Hirayama et al : Famotidine-induced acute interstitial nephritis, Nephrol Dial Transplant. 1998 Oct;13(10):2636-8.
(12)廣岡賢輔ほか:ファモチジン中止で振戦の軽減した1例, 日本医療薬学会年会講演要旨集 (suppl.1): 434-434, 2014.
(13)P O Katz et al : Relationship between intragastric acid control and healing status in the treatment of moderate to severe erosive oesophagitis, Aliment Pharmacol Ther. 2007 Mar 1;25(5):617-28.
(14)F W Green Jr et al : Effect of acid and pepsin on blood coagulation and platelet aggregation. A possible contributor prolonged gastroduodenal mucosal hemorrhage, Gastroenterology. 1978 Jan;74(1):38-43.
(15)ガスター錠 添付文書
(16)Thomas E Lackner et al : Gastrointestinal disease control after histamine2-receptor antagonist dose modification for renal impairment in frail chronically ill elderly patients, J Am Geriatr Soc. 2003 May;51(5):650-6.
(17)Nolly RJ, Skoutakis VA. Cost considerations of intravenously administered histamine2-receptor antagonists. DICP 1989; 23 : S23–S28



